Хроническая радикулопатия: новые возможности терапии
Данилов А.Б., Жаркова Т.Р.
Компрессия нервного корешка (радикулопатия) занимает от 8 до 10% среди других причин болей в спине [1-4,9]. До 90% радикулопатий обусловлено грыжами межпозвонковых дисков, и более чем в 80% случаев патология выявляется в поясничном отделе. В 48% случаев грыжи локализуются на уровне L5-S1 пояснично-крестцового отдела, в 46% случаев - на уровне L4-L5; остальные 6% на других уровнях или на нескольких уровнях пояснично-крестцового отдела. У 80% боли проходят под влиянием лечения в достаточно короткий срок - от нескольких недель до месяца, однако у остальных 20% пациентов приобретают хроническое рецидивирующее течение [14]. Наиболее часто это заболевание встречается в возрасте от 45 до 64 лет.
С точки зрения механизмов боли радикулопатию сегодня рассматривают, как смешанный болевой синдром, где присутствуют как ноцицептивный, так и нейропатический компоненты [2,5,8]. Этот подход позволяет проводить дифференцированную фармакотерапию боли в зависимости от выраженности того или иного компонента. Для терапии ноцицептивного компонента рекомендуется использовать простые анальгетики или нестероидные противовоспалительные препараты (НПВП), которые, как известно, хорошо купируют ноцицептивную боль. В фармакотерапии нейропатической боли наиболее часто используют антиконвульсанты, антидепрессанты и опиоидные анальгетики [2]. Антиконвульсанты чаще применяются для купирования нейропатической боли жгучего и "стреляющего" характера. Одним из таких антиконвульсантов, наиболее признанных и апробированных в мире, является габапентин [6,12,13,16]. Механизм его действия связан с влиянием на центральные механизмы боли на уровне заднего рога. Действуя на специальную альфа-2-субъединицу кальциевых каналов на пресинпатической мембране в терминали сенсорного нейрона, габапентин блокирует поступление кальция в клетку и тем самым затрудняет выброс болевых медиаторов (глутамата, субстанции Р) в синаптическую щель. Это нарушает передачу болевых сигналов с периферического нейрона на центральный. В результате происходит уменьшение центральной сенситизации, улучшение нейромедиаторного баланса в сторону усиления противоболевых ГАМК-эргических влияний и редукции эффектов глутамата, главного нейротрансмиттера боли [16].
С целью дифференцированного лечения болевого синдрома при радикулопатии очень важно оценить представленность ноцицептивного и нейропатического механизмов боли в каждом конкретном случае. Для оценки достоверности наличия нейропатической боли разработан ряд опросников. Опросник DN4 состоит из 10 пунктов, касающихся характерных клинических характеристик нейропатической боли [7]. В результате анкетирования и неврологического анализа определяется суммарный балл (от 0 до 10). Боль оценивают как нейропатическую при сумме баллов не менее 4. Опросник PainDETECT объединяет в себе схему распределения болевых расстройств в виде картинки со шкалой ВАШ и опросником, направленным на выявление спонтанных и вызванных симптомов нейропатической боли [11]. Также при помощи рисунка оценивается характер течения боли. Опросник наиболее полно отражает все возможные параметры боли и позволяет наглядно отслеживать картину болевого синдрома в динамике. Сумма баллов более 19 означает вероятное наличие у пациента нейропатического компонента боли. От 13 до 18 баллов - показания неоднозначны, однако болевой компонент может иметь место.
Целью настоящего исследования была оценка болевого синдрома при хронической радикулопатии с точки зрения выраженности нейропатического компонента боли и оценка клинической эффективности препарата Тебантин (габапентин) для целенаправленной терапии этого компонента.
Материал исследования
Группу пациентов составили 37 человек с хронической пояснично-крестцовой радикулопатией (женщин - 59%, мужчин - 41%). Критериями включения являлись: хронический болевой синдром на фоне дискогенной радикулопатии L4-L5, L5-S1 (длительностью не менее 3 мес). Каждый пациент был информирован о цели приема препарата, возможных побочных эффектах терапии, подписав информированное согласие. Средний возраст пациентов, получавших терапию, составил 47,62±13,36 лет.
Методы исследования
Клинико-неврологическое обследование включало в себя сбор анамнеза заболевания, общесоматический и неврологический осмотр. Для подтверждения наличия грыжи межпозвонкового диска на уровне L4-L5 и/или L5-S1 всем пациентам проводилась магнитно-резонансная томография.
На каждого больного оформлялась клиническая анкета, включающая паспортную часть, описание субъе-ктивных характеристик (дескрипторов) болевого синдрома, оценивалась интенсивность каждого дескриптора по визуальной аналоговой шкале, локализация боли, длительность болевого синдрома, количество обострений в анамнезе, течение заболевания, провоцирующие факторы и связь с физической нагрузкой, сопровождающие симптомы, меры купирования боли, а также жалобы в межприступный период и сопутствующие заболевания. В неврологическом статусе оценивались локализация и характер чувствительных нарушений. Учитывалось также наличие или отсутствие феноменов стимулзависимой болевых симптомов: аллодинии, гипералгезии, парестезий и дизестезии. Чувствительные нарушения фиксировались на картинке в анкете пациента. Оценивались сухожильные рефлексы, сила в конечностях. Согласно опроснику Хабирова вычислялся индекс мышечно-тонического синдрома [4].
Психометрическое тестирование включало в себя оценку выраженности депрессии по опроснику Бека, оценку уровня реактивной и личностной тревожности по Спилбергеру и оценку качества жизни по опроснику SF36.
Лечение проводилось по следующей схеме. Монотерапия Тебантином в дозе 1800 мг в сутки (по 600 мг 3 раза) в течение 6 недель с предварительным титрованием: в первые сутки - 300 мг/сут.; во 2-е - 600, на 3-и - 900, на 4-6-е - 1200, на 7-10-е - 1500 и с 11 суток - 1800 мг/сут. в три приема по 600 мг. Проводилась оценка интенсивности болевого синдрома по визуально-аналоговой шкале (от 0 до 10) на каждой неделе лечения, а также оценка достоверности наличия нейропатического компонента болевого синдрома по опросникам DN4 и PainDetect до и после лечения.
Результаты
Длительность заболевания в среднем по группе составила 3,4±3,9 года и колебалась от 6 месяцев до 18 лет. Средний возраст дебюта заболевания составил 44,1±12,7, у мужчин болевой синдром впервые выявлялся в возрасте 40,3±11,5 лет, у женщин - в возрасте 46,6±13,1 лет. Количество обострений в группе обследованных за период заболевания составило 2,9±2,3.
Были выявлены 4 разновидности течения болевого синдрома среди пациентов. Непрерывная боль, немного меняющаяся по интенсивности, отмечена у 8 пациентов (21,6%). Непрерывная боль с периодическими, редкими приступами, выявлена у 6 пациентов (16,2%). 9 пациентов (24,4%) характеризовали течение своего болевого синдрома, как приступы боли без болевых ощущений между ними. Наиболее часто - у 14 пациентов (37,8%) отмечены частые приступы боли, сопровождающиеся болевыми ощущениями в промежутках между ними.
Все обследованные пациенты отмечали возникновение приступов боли в разное время суток. 7 пациентов (19%) указывали на то, что приступы боли возникают исключительно в ночное время, 18 пациентов (49%) предъявляли жалобы на боли, возникающее только днем, и 12 пациентов (32%) отмечали возникновение боли как в дневные, так и в ночные часы.
Значительная группа пациентов - 26 человек (70,2%) указывали на то, что физическая нагрузка усиливает выраженность болевого синдрома. 4 пациента (10,8%) считали переохлаждение фактором, провоцирующим болевой синдром. 16 пациентов (43,2%) отмечали возникновение боли при ходьбе, 11 человек (29,8%) - в положении сидя.
По данным клинико-неврологического осмотра и на основании субъективных жалоб пациентов было выявлено: жалобы на стреляющую боль предъявляли 23 пациента (62%), жгучую боль - 20 пациентов (54%), сжимающую боль - 24 пациента (65%), ноющую - 12 (62%), аллодиния выявлена у 16 (43,2%), парестезии - у 29 пациентов (78%).
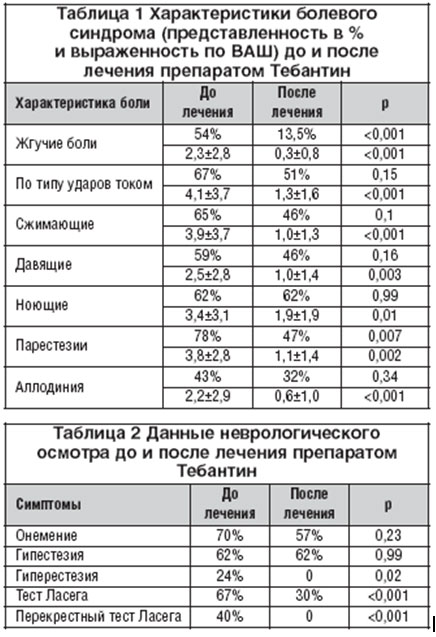
В таблице 1 указаны характеристики болевого синдрома до и после лечения препаратом Тебантин. Отмечалось достоверное снижение интенсивности жгучей, сжимающей, давящей, ноющей боли, боли по типу ударов током, достоверное снижение частоты жгучей боли на фоне лечения. Отмечено уменьшение интенсивности аллодинии, частоты и интенсивности парестезии.
Жалобы на онемение предъявляли 26 пациентов (70%). Гипалгезия выявлена у 23 пациентов (62%), у 11 пациентов отмечалось снижение болевой чувствительности в зоне иннервации корешка L5-S1, у 11 пациентов - в зоне иннервации корешка L4-L5, у 1 пациента - в зоне иннервации корешков L4-L5 и L5-S1. Гипералгезия отмечалась у 9 пациентов (24%), у 4 человек - в зоне иннервации корешка L5-S1, у 5 - в зоне иннервации корешка L4-L5.
Положительный тест Ласега выявлен у 67% пациентов, перекрестный тест Ласега - у 40%. В таблице 2 указаны данные неврологического осмотра пациентов до и после лечения. Отмечено достоверное снижение частоты гиперестезии, частоты встречаемости теста Ласега и перекрестного теста Ласега на фоне лечения.
Снижение коленного рефлекса отмечено у 6 пациентов (16,2%), коленный рефлекс отсутствовал у 3 пациентов (8%). Снижение ахиллова рефлекса выявлено у 5 пациентов (13,5%), его отсутствие - у 25 пациентов (67,5%).
Среди обследованной группы пациентов проводился анализ напряжения многораздельных мышц спины и мышцы, выпрямляющей позвоночник. Производилась пальпация мышц на поясничном уровне при наклоне пациента вперед на 10-15°. При пальпации проводились оценка выраженности спонтанной боли, тонуса, болезненности мышц, продолжительности болезненности и степени иррадиации боли при пальпации. Согласно опроснику Хабирова вычислялся индекс мышечно-тонического синдрома. У 12 пациентов (32,4%) отмечалась первая степень мышечно-тонического синдрома, у 25 пациентов (67,6%) - вторая степень мышечно-тонического синдрома. Выраженных проявлений мышечно-тонического синдрома у пациентов с хронической болью при пояснично-крестцовой радикулопатии обнаружено не было.
По данным опросника DN4 средний балл составил 5,45±1,57, у 90% пациентов ?4; по данным PainDETECT - 13,78±3,10, у 65% пациентов ?13 (рис. 1). Выраженность боли по ВАШ среди пациентов обследованной группы - 7,45±1,83. Динамика ВАШ на фоне лечения препаратом Тебантин по неделям указана на рисунке 2. Достоверное уменьшение болевого синдрома по ВАШ отмечено уже на 3-й неделе лечения.
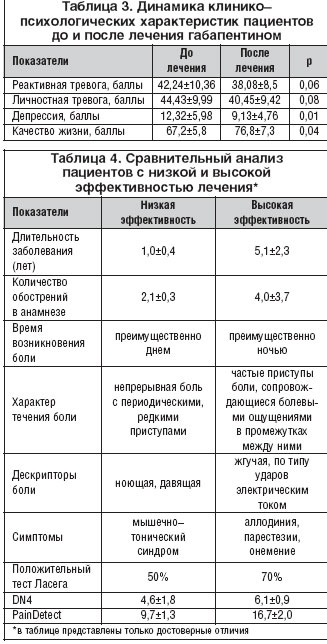
Динамика клинико-психологических характеристик пациентов до и после лечения Тебантином представлена в таблице 3.
Отмечалось достоверное уменьшение выраженности депрессии и достоверное улучшение качества жизни пациентов на фоне лечения.
Переносимость препарата у большинства пациентов была удовлетворительной, 5 пациентов в течение первых 4-5 дней приема испытывали легкую сонливость и небольшое головокружение.
Для анализа предикторов эффективности лечения оценивались две полярные группы пациентов: с низкой эффективностью лечения и высокой эффективностью лечения относительно данных ВАШ (табл. 4).
Лечение Тебантином было наиболее эффективно у пациентов, имеющих большую длительность заболевания и большее количество обострений в анамнезе. У пациентов этой группы боль чаще возникала в ночное время, по течению это были частые приступы боли, сопровождающиеся болевыми промежутками между ними. Пациенты с более высокой эффективностью лечения изначально достоверно чаще предъявляли жалобы на стреляющую, жгучую боль, у них чаще встречались такие симптомы, как аллодиния, парестезии, онемение, положительный симптом Ласега. Наблюдалось более эффективное лечение у пациентов с изначально более высокими баллами по данным опросников DN4 и PainDETECT.
Обсуждение
В настоящее время рассматриваются несколько механизмов формирования боли при компрессионной радикулопатии [10]. Помимо непосредственной механической компрессии корешка, источником боли могут быть повреждения ноцицепторов самого межпозвонкового диска. Кроме того, определенную роль играет воспалительный процесс, когда медиаторы воспаления, локально воздействуя на нервные окончания в тканях, также участвуют в генерации болевых ощущений. Таким образом, боль при радикулопатии принято считать смешанной, где присутствуют ноцицептивный и нейропатический компоненты [8,10]. Крупные эпидемиологические исследования свидетельствуют о том, что у 20-35% пациентов с дискогенной радикулопатией преобладает нейропатический компонент [10]. Причиной формирования нейропатического компонента может быть механическая компрессия нервного корешка (механическая нейропатия) и/или раздражение его под влиянием медиаторов воспаления (воспалительная нейропатия) [10]. Специфическими характеристиками нейропатического компонента при болях в спине являются жалобы на стреляющую, глубокую мучительную, тянущую, ноющую, сверлящую боль, жжение, аллодиния, симптом Ласега, болезненное онемение [15].
По данным нашего исследования, нейропатический компонент выявлен у 90% пациентов по данным опросника DN4 и у 65% пациентов по данным опросника PainDETECT, что подтверждает данные о том, что болевой синдром при радикулопатии является смешанным, при ведущей роли нейропатического компонента. Следует отметить, что в нашем исследовании опросник DN4 оказался более информативным и чувствительным в диагностике нейропатического компонента боли, чем опросник PainDETECT.
Использование препарата Тебантин в нашем исследовании преследовало цель уточнения механизмов боли при радикулопатии и возможности целенаправленного терапевтического воздействия на него.
Результаты работы показали высокую эффективность габапентина (Тебантина) в отношении редукции именно нейропатического компонента боли. Это, с одной стороны, свидетельствует о том, что в формировании боли при радикулопатии нейропатический компонент играет существенную роль, а с другой - указывает на возможность эффективного воздействия на этот компонент с помощью габапентина (Тебантина). Следует подчеркнуть, что в результате уменьшения боли отмечено достоверно улучшение психологического статуса (уменьшение депрессии и тревоги).
Таким образом, диагностика нейропатического компонента при болях в спине имеет важное значение с точки зрения дифференцированной фармакотерапии. Препарат Тебантин оказывает отчетливое положительное действие преимущественно на нейропатический компонент в структуре смешанного болевого синдрома при хронической радикулопатии и в меньшей степени влияет на характеристики ноцицептивного компонента.
Результаты проведенного исследования позволяют сделать вывод о целесообразности уточнения выраженности ноцицептивного и нейропатического компонентов при болях в спине для выбора адекватного препарата из группы НПВП для воздействия на ноцицептивный компонент и габапентина для лечения нейропатического компонента. Вполне вероятно, что в большинстве случаев хронической радикулопатии необходимо одновременное назначение НПВП и габапентина в адекватном соотношении для воздействия на оба компонента болевого синдрома, что может положительно повлиять на эффективность и сроки проведения фармакотерапии и реабилитации.

Литература
1. Болевые синдромы в неврологической практике//Под ред. Вейна А.М. - М.:МЕДпресс-информ, 2001.
2. Данилов А.Б., Давыдов О.С. Нейропатическая боль, 2007
3. Подчуфарова Е.В, Хронические боли в спине: патогенез, диагностика, лечение.// РМЖ.- 2003. - Т. 11.- № 25.- С. 32-37
4. Хабиров Ф.А. Руководство по клинической неврологии позвоночника. Казань, 2006.
5. Baron R., Binder A. How neuropathic is sciatica? The mixed pain concept. Orthopade., 2004 May; 33(5):568-75.
6. Birklein F. Mechanism-based treatment principles of neuropathic pain. Fortschr Neurol Psychiatr., 2002 Feb; 70(2):88-94.
7. Bouhassira D, Attal N, Alchaar H, Boureau F, Brochet B, Bruxelle J, Cunin G, Fermanian J, Ginies P, Grun-Overdyking A, Jafari-Schluep H, Lanteri-Minet M, Laurent B, Mick G, Serrie A, Valade D, Vicaut E.Comparison of pain syndromes associated with nervous or somatic lesions and development of a new neuropathic pain diagnostic questionnaire (DN4). Pain. 2005 Mar; 114(1-2):29-36.
8. Brisby H. Pathology and possible mechanisms of nervous system response to disc degeneration. J Bone Joint Surg Am. 2006 Apr; 88 Suppl 2:68-71.
9. Deyo RA, Tsui-Wu YJ. Descriptive epidemiology of low-back pain and its related medical care in the United States. Spine (Phila Pa 1976). 1987 Apr; 12(3):264-8.
10. Freynhagen R, Baron R. The evaluation of neuropathic components in low back pain. Curr Pain Headache Rep. 2009 Jun; 13(3):185-90.
11. Freynhagen R, Baron R, Gockel U, Tolle TR. painDETECT: a new screening questionnaire to identify neuropathic components in patients with back pain. Curr Med Res Opin. 2006 Oct; 22(10):1911-20.
12. Hansson P., Fields H., Hill R., Marchettini P., eds. Neuropathic Pain: Pathophysiology and Treatment, Progress in Pain Research and Management. Vol. 21. Seattle, WA: IASP Press; 2001: 151-167.
13. Junker U., Brunnmuller U. Efficacy and tolerability of gabapentin in the treatment of patients with neuropathic pain. Results of an observational study involving 5620 patients. MMW Fortschr Med., 2003; 145:37.
14. Manchikanti L, Singh V, Datta S, Cohen SP, Hirsch JA; Comprehensive review of epidemiology, scope, and impact of spinal pain. 2009 Jul-Aug;12(4):E35-70. 2005 Mar; 114(1-2):29-36.
15. Оostdam EM, Duivenvoorden HJ Description of pain and the degree to which the complaints fit the organic diagnosis of low back pain. Pain. 1984 Jan; 18(1):71-82.
16. Wiffen PJ, Collins S. Аnticonvulsant drugs for acute and chronic pain (Review). The Cochrane Collaboration, 2008; 1-35.
Ключевые слова статьи: Хроническая, радикулопатия, новые, возможности, терапии
Источник РМЖ 26 января 2010 г, том 18, № спец













