Диагностика и лечение неврологических проявлений остеохондроза позвоночника
О.С.Левин
Кафедра неврологии РМАПО, Москва
Боль в спине – одна из наиболее актуальных проблем здравоохранения. В течение жизни она возникает у 70–90% населения и ежегодно отмечается у 15–25% [1]. Хотя эпизод боли в спине часто оказывается кратковременным, примерно у трети пациентов в последующем развивается хроническая боль, которая сохраняется более 12 нед и служит причиной длительной нетрудоспособности у 4% населения [2–4].
На протяжении десятилетий в отечественной клинической практике универсальной причиной боли в спине считался остеохондроз позвоночника. Между тем выявляемые с помощью спондилографии, компьютерной (КТ) или магнитно-резонансной (МРТ) томографии дегенеративно-дистрофические изменения позвоночника, считавшиеся маркерами остеохондроза, плохо коррелируют с клинической картиной и часто встречаются у лиц, не страдающих болью в спине [5]. Таким образом, сам по себе дегенеративный процесс в позвоночнике может считаться лишь предпосылкой боли в спине, но не ее непосредственной причиной. К сожалению, упрощенное понимание проблемы остеохондроза позвоночника препятствует попыткам выяснения истинных причин боли в спине и разработке дифференцированных подходов к ее лечению. В данной статье рассматриваются вопросы диагностики и дифференцированного лечения различных вертеброневрологических синдромов, возникающих на фоне дегенеративных изменений в пояснично-крестовом отделе. Однако аналогичный подход может быть распространен и на патологию шейного отдела позвоночника.
Основные причины боли в спине при остеохондрозе позвоночника
Согласно современным представлениям остеохондроз позовночника представляет собой весьма сложный каскадный процесс. Его отправной точкой, как правило, служат дегенеративные изменения в межпозвонковых дисках, которым способствуют повторные травмы, избыточная статическая или динамическая нагрузка, наследственная предрасположенность. Межпозвонковый диск постепенно теряет воду, ссыхается, утрачивает амортизирующую функцию и становится более чувствительным к механической нагрузке. Фиброзное кольцо, расположенное по периферии диска, истончается, в нем появляются трещины, по которым центральная часть диска – пульпозное ядро – смещается к периферии, формируя протрузию (выпячивание).
Вследствие травмы или интенсивной нагрузки протрузия может скачкообразно увеличиваться, что приводит к выпячиванию пульпозного ядра и части фиброзного кольца в позвоночный канал, которое обозначают как грыжа диска. Грыжа обычно представляет собой солидное образование, сохраняющее связь с телом диска, но иногда ее фрагменты выпадают в позвоночный канал.
Боль при грыже диска впервые появляется в связи с раздражением болевых рецепторов наружных слоев фиброзного кольца и задней продольной связки, импульсация от которых поступает в спинной мозг по ветвям синувертебрального нерва. Рефлекторно возникает спазм сегментарных мышц, имеющий защитный характер и приводящий к иммобилизации пораженного сегмента (миофиксация), но со временем он утрачивает саногенную роль и становится самостоятельным фактором, поддерживающим боль [6]. Смещаясь в сторону позвоночного канала или межпозвонкового отверстия, грыжа может компримировать прилегающий спинномозговой корешок и соответствующий спинномозговой ганглий, что ведет к возникновению корешкового синдрома (радикулопатии). Повреждение корешка бывает обусловлено не только его механическим сдавлением, но также воспалением, отеком и демиелинизацией, в генезе которых определенная роль может принадлежать иммунологическим процессам [7].
Еще на более раннем этапе дегенеративного процесса постепенное снижение высоты диска нарушает функционирование всего позвоночно-двигательного сегмента (ПДС), включающего два смежных позвонка, соединенных межпозвонковым диском спереди и 2 межпозвонковыми (фасеточными) суставами сзади, с окружающими их мышцами и связками. Суставные фасетки в межпозвонковых суставах "наезжают" друг на друга, что может приводить к подвывиху и смещению позвонков относительно друг друга (спондилолистезу). Возникающая в итоге нестабильность ПДС повышает чувствительность позвоночника к травме или резким движениям, ускоряет дегенеративные изменения, прежде всего артроз фасеточных суставов. Эти изменения часто остаются асимптомными, но при травме или избыточной нагрузке они способны стать источником боли [2, 8].
Важную роль в генезе боли играет формирование обратимой блокады ("болезненной дисфункции") ПДС, что клинически проявляется ограничением подвижности позвоночника, локальными и отраженными болями, дистрофическими изменениями соединительно-тканных структур (сегментарным "целлюло-тено-периостео-миалгическим синдромом") [6, 9].
С годами механическая стабильность ПДС и всего позвоночника восстанавливается за счет краевых разрастаний (остеофитов), фиброза дисков и капсулы, анкилоза фасеточных суставов, утолщения связок. Эти изменения завершают "дегенеративный каскад" в позвоночнике и иногда приводят к спонтанному стиханию боли. Но одновременно они способны вызвать стеноз позвоночного канала. Кроме того, остеофиты, направленные в сторону спинномозгового канала, могут травмировать корешки, вызывая тем самым стойкий болевой синдром.
Таким образом, на различных этапах дегенеративного процесса в позвоночнике ведущую роль в развитии болевого синдрома играют различные факторы – грыжа диска, нестабильность или блокада ПДС, артроз фасеточных суставов и стеноз позвоночного канала (рис. 1). В каждом из этих случаев болевой синдром имеет клиническое своеобразие, различную временную динамику, прогноз, и требует особого подхода к лечению [10]. В большинстве случаев боль в спине и нижних конечностях носит ноцицептивный местный или отраженный характер, лишь в сравнительно небольшом числе случаев она объясняется повреждением спинномозгового корешка или ганглия и имеет невропатический характер.
Дискогенный болевой синдром
Патология межпозвонкового диска – причина примерно 30% случаев боли в спине. Это основная причина хронической боли в спине у лиц молодого возраста (30–50 лет). В большинстве случаев поражаются два последних диска: LV–SI и LIV–LV, реже LIII–LIV. Для характеристики степени выпячивания диска многие авторы используют термины: "протрузия", "грыжа", "пролапс", в которые, однако, вкладывают неодинаковый смысл. Некоторые авторы применяют их практически как синонимы. Другие предлагают использовать термин "протрузия" для обозначения начальной стадии выпячивания диска, когда пульпозное ядро еще не прорвало наружные слои фиброзного кольца, термин "грыжа" – только в том случае, когда пульпозное ядро или его фрагменты прорвали наружные слои фиброзного кольца, а термин "пролапс" – для обозначения выпадения грыжевого материала, утратившего связь с диском, в позвоночный канал. Третьи авторы предлагают выделять интрузии, при которых наружные слои фиброзного кольца остаются интактными, и экструзии, при которых грыжевой материал прорывается через наружные слои фиброзного кольца и заднюю продольную связку в позвоночный канал.
Во избежание путаницы далее мы будем использовать термин "грыжа диска" для обозначения любого выпячивания диска за линию, соединяющую края соседних позвонков, которое превышает физиологические пределы (в норме не более 3 мм).
Болевые синдромы обычно вызываются задними грыжами диска [2, 6, 11].
Начальные фазы формирования грыжи диска сопровождаются локальной и рефлекторной болью, нередко иррадиирующей в крестцово-подвздошное сочленение, крестец, копчик, мошонку или промежность, для более поздней фазы характерна корешковая боль. Следует особо отметить, что причиной как острого, так и, что особенно важно, хронического дискогенного болевого синдрома может быть не только грыжа диска, но и вклинивание фрагмента ядра диска в радиальную трещину фиброзного кольца с перерастяжением наружных слоев кольца без существенного выпячивания всего диска кзади [3, 4].
Дискогенная боль, не связанная с компрессией корешка, максимально выражена в пояснице, но часто распространяется в ягодицу и бедро. Для нее характерен ряд признаков, отличающих ее от рефлекторной боли иного происхождения. Дискогенная боль бывает постоянной или перемежающейся и обычно усиливается при сгибании и сидении, тогда как при разгибании может как усиливаться, так и ослабляться. При упражнениях на разгибание можно отметить феномен "централизации" боли, которая ослабляется в ноге, но усиливается в поясничной области [5, 7].
Боль нередко усиливается при натуживании, кашле и чиханьи, надавливании на яремные вены. В покое она обычно ослабевает, особенно если больной лежит на здоровом боку, согнув больную ногу в коленном и тазобедренном суставах. При осмотре спина часто бывает фиксирована в слегка согнутом положении, наклон кпереди и в больную сторону ограничен, отмечается выраженное напряжение паравертебральных мышц, уменьшающееся в положении лежа, часто выявляется сколиоз, усиливающийся при наклоне кпереди, но пропадающий в положении лежа; при боковой грыже сколиоз направлен в здоровую сторону, при парамедианной – в больную. Боль при грыже диска часто сопровождается формированием на периферии (в мышцах ягодицы, бедра, голени) болезненных и триггерных точек, которые могут играть самостоятельную роль в поддержании болевого синдрома.
Подтвердить наличие грыжи диска и уточнить ее степень можно с помощью нейровизуализационных методов (КТ, МРТ, миелография). Вместе с тем следует подчеркнуть, что диагностика грыжи диска как причины болевого или корешкового синдрома возможна лишь в том случае, когда клиническая картина соответствует уровню и степени выпячивания диска. Обычно выпячивание диска считается клинически значимым, если превышает 25% переднезаднего диаметра позвоночного канала (примерно 10 мм).
Подтверждение дискогенного характера боли возможно при дискографии, проводимой под флюороскопическим контролем, – стимуляция пораженного диска индуцирует боль с характерной для данного пациента иррадиацией.
Наиболее сложная задача – диагностировать внутренний разрыв диска с внедрением пульпозного ядра в трещину фиброзного кольца. Его не удается выявить при миелографии, а также на аксиальных изображениях диска, получаемых с помощью КТ или МРТ. Лишь на сагиттальных Т2-взвешенных МР-изображениях в этих случаях можно отметить зону высокой интенсивности сигнала в проекции фиброзного кольца (рис. 2) или изменения концевых пластинок, однако окончательно подтвердить диагноз можно лишь с помощью КТ-дискографии.
Болезненная дисфункция ПДС
Дегенерация диска может приводить не только к грыже, но и к равномерной умеренной протрузии диска, уменьшению его высоты и изменению взаиморасположения основных элементов ПДС. Это может быть причиной нестабильности или патологической фиксации сегмента, приводящих к хроническому болевому синдрому. Причиной нестабильности может быть также спондилолистез и другие заболевания позвоночника.
Нестабильность ПДС приводит к избыточной нагрузке на фасеточные суставы и мышцы. Боль, связанная с ней, обычно двусторонняя, усиливается при длительном пребывании в одном положении, наклонах, поднятии тяжести. Движения в позвоночнике обычно не ограничены, но болезненны (особенно разгибание). Поясничная боль иногда иррадиирует в крестцово-подвздошное сочленение и крыло подвздошной кости, но не в ягодицу или бедро. Диагноз может быть подтвержден с помощью функциональной рентгенографии позвоночника.
Артроз межпозвонковых (фасеточных) суставов
Артроз межпозвонковых (фасеточных) суставов (спондилоартроз) является причиной боли в спине примерно в 20% случаев. У пожилых (в возрасте старше 65 лет) спондилоартроз – самая частая причина хронической боли в спине, на долю которой приходится до 40% случаев. Спондилоартроз может возникать: 1) в результате перегрузки задних отделов ПДС (например, в связи с нарушением статики позвоночника), 2) при распространенном остеоартрозе, поражающем суставы позвоночника и конечностей, 3) вследствие дегенерации и уменьшения высоты диска, приводящих к изменению взаимоотношений суставных отростков, и сопровождаться функциональной блокадой суставов, подвывихом в суставах с ущемлением суставной капсулы, воспалением суставных тканей [5].
Клинически спондилоартроз проявляется двусторонней болью, которая в отличие от дискогенной боли обычно локализуется паравертебрально, а не по средней линии. Боль максимально выражена в пояснице, но нередко иррадиирует в крестцово-подвздошное сочленение, ягодицу, бедро, возможно и более дистальное распространение боли вплоть до стопы (рис. 3). Как правило, она имеет интермиттирующий характер и усиливается при длительном стоянии и разгибании, особенно при одновременной ротации (хотя это не абсолютный признак!), но уменьшается или по крайней мере не усиливается при наклоне вперед, сидении и ходьбе, а также в положении лежа на спине [12].
Рентгенография при спондилоартрозе выявляет сужение межсуставных щелей, субхондральный склероз, деформацию и гипертрофию суставных фасеток вследствие костно-хрящевых разрастаний, но нередко подобные изменения не сопровождаются какой-либо симптоматикой. Поэтому наиболее достоверный признак – уменьшение боли при двусторонней блокаде межпозвонковых суставов или иннервирующих их медиальных волокон дорсальных ветвей спинномозговых нервов местным анестетиком.
Синдром крестцово-подвздошного сочленения
Синдром крестцово-подвздошного сочленения (сакроилеит) проявляется болью в области сочленения, иррадиирующей в пах, большой вертел, ягодицу. При осмотре можно выявить болезненность в области сочленения при пальпации, боковом давлении на таз, отведении бедра против сопротивления, переразгибании или наружной ротации бедра. Боль усиливается при ходьбе, наклонах, длительном пребывании в положении сидя или стоя. Его развитию способствуют укорочение ноги, травмы, беременность. По некоторым данным, синдром крестцово-подвздошного сочленения выявляется примерно в 15% случаев хронической боли в спине. Но в то же время следует учитывать, что нередко сочленение служит проекцией отраженных, болей при грыже диска (особенно при компрессии корешка S1). Наиболее значимый диагностический тест, позволяющий связать боль в спине с патологией сочленения, – исчезновение боли после блокады сочленения, проводимой под флюороскопическим контролем. Истинный сакроилеит, сопровождающийся характерными рентгенологическими изменениями, является одним из основных признаков анкилозирующего спондилита [5].
Радикулопатии
Хотя термин "радикулит" глубоко укоренился в бытовом сознании населения практически как синоним боли в спине, на практике корешковый синдром выявляется примерно лишь в 10% случаев боли в спине. Его самая частая причина – грыжа межпозвонкового диска, но он может быть также связан со стенозом межпозвонкового отверстия или позвоночного канала [3, 5, 8].
При радикулопатиях боль преимущественно ощущается в конечности и иррадиирует в дистальную часть зоны иннервации соответствующего корешка. Боль, ограничивающаяся областью спины, исключает корешковое поражение. На практике нередки затруднения при дифференциальной диагностике корешкового синдрома, сопровождающегося невропатической болью, и рефлекторной люмбоишиалгии, представляющей собой разновидность отраженной ноцицептивной боли. Их сравнительная характеристика дана в табл. 1.
Симптомы натяжения неспецифичны для корешкового поражения, но пригодны для оценки тяжести и динамики вертеброгенного болевого синдрома. При грыже диска поражение корешка может быть следствием механического сдавления, ишемии, отека, воспаления, демиелинизации и аксональной дегенерации. У пожилых радикулопатия часто бывает результатом сдавления корешка не грыжей диска, а суставной фасеткой (при артропатии межпозвонковых суставов), остеофитом или гипертрофированной желтой связкой.
Стеноз позвоночного канала
Стеноз позвоночного канала может быть врожденным, приобретенным или комбинированным. Приобретенный стеноз бывает следствием спондилолистеза, грыжи межпозвонковых дисков, образования задних остеофитов, гипертрофии связок, спондилоартроза с гипертрофией суставных фасеток, травмы позвоночника, гипертрофии и оссификации задней продольной связки. Стеноз позвоночного канала на грудном и поясничном уровне диагностируют, если переднезадний диаметр позвоночного канала менее 12 мм либо площадь канала менее 100 мм2. Стеноз поясничного отдела позвоночного канала приводит к компрессии корешков конского хвоста и питающих его сосудов. Его основное клиническое проявление – нейрогенная (каудогенная) перемежающаяся хромота. Она выражается в появлении при ходьбе или длительном стоянии двусторонних болей, онемения, парестезий, слабости в мышцах голени, реже бедра, которые уменьшаются в течение нескольких минут, если больной наклонится кпереди или сядет. На долю стеноза позвоночного канала приходится около 5% случаев боли в спине.
Миофасциальный синдром
Миофасциальный синдром в паравертебральных мышцах может развиваться на фоне дегенеративного процесса в позвоночнике или независимо от него в связи с длительным пребыванием в нефизиологической позе, хронической микротравматизацией, перегрузкой, перерастяжением или сдавлением мышц, травмой, длительной иммобилизацией. В основе миофасциального синдрома лежит формирование в мышцах триггерных точек, раздражение которых вызывает не только локальную, но и отраженную боль (в удаленной от этой точки зоне). Миофасциальный синдром в малой ягодичной и грушевидной мышцах может имитировать вертеброгенную некорешковую люмбоишиалгию (рис. 4). Триггерной точке соответствует зона локального мышечного уплотнения, пальпация которой не только воспроизводит боль, которую испытывает больной, но и вызывает локальное мышечное сокращение. Инактивация активных миофасциальных зон путем инъекции в них местного анестетика с последующим пассивным растяжением мышц приводит к купированию болевого синдрома.
Синдром грушевидной мышцы
Синдром грушевидной мышцы встречается редко и может иметь как вертеброгенную, так и невертеброгенную природу. Он характеризуется сдавлением седалищного нерва воспаленной или укороченной грушевидной мышцей либо ее сухожилием. Сдавление усиливается при внутренней ротации бедра. Синдром проявляется болью в ягодичной области, иррадиирующей по задней поверхности бедра и голени. Возможны легкая слабость сгибателей голени и парез стопы, снижение чувствительности в нижней части голени и по наружному краю стопы, снижение или выпадение ахиллова рефлекса, вегетативные расстройства на голени и стопе. В диагностике важнее значение имеет тот факт, что нерв сдавливается ниже места отхождения нервных ветвей к средней и малой ягодичным мышцам и мышце, натягивающей широкую фасцию бедра, поэтому электромиелография выявляет интактность этих мышц, но денервацию большой ягодичной мышцы и других мышц ноги. Блокада мышцы, специальные упражнения, ультразвук или фонофорез с гидрокортизоном уменьшают мышечный спазм и ведут к ослаблению болей [2].
Рис. 1. Каскад дегенеративных изменений при остеохондрозе позвоночника и механизмы развития болевого синдрома.
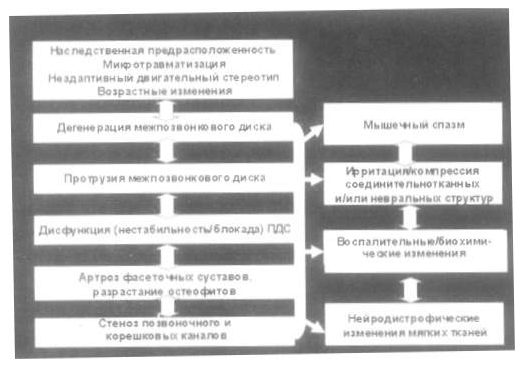
Рис. 2. МРТ поясничного отдела позвоночника. Грыжа диска.
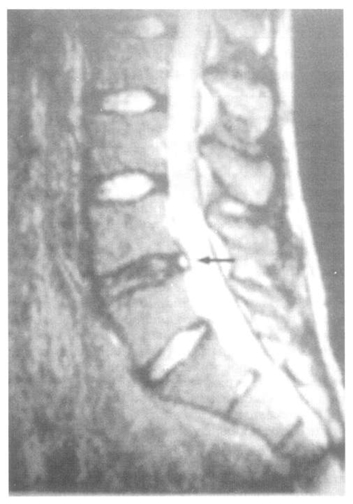
Рис. 3. Локализация боли при спондилоартрозе.
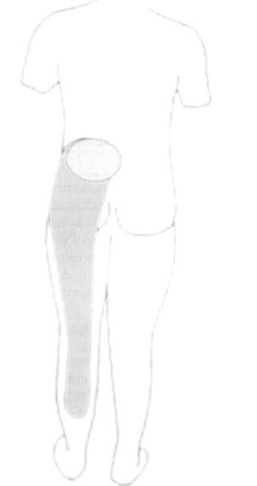
Таблица 1. Сравнительная характеристика корешкового синдрома и рефлекторной люмбоишиалгии
|
Признаки |
Корешковый синдром |
Рефлекторная люмбоишиалгия |
|
Характер боли |
Интенсивная стреляющая или пронизывающая |
Постоянная ноющая, часто глубинная |
|
Локализация боли |
Часто односторонняя, имеет четкие границы, иррадиирует по дерматому, обычно в его дистальную часть; может"метаться" по конечности |
Часто двусторонняя, диффузная, не имеет четких границ, иррадиирует по миотому или склеротому, максимально выражена в области ягодиц и бедер, но иногда "опускается" и ниже колена; установившаяся боль редко меняет локализацию, но может варьировать по интенсивности |
|
Симптомы натяжения |
Выражены |
Могут присутствовать |
|
Сухожильные рефлексы |
Снижены или выпадают в зоне иннервации корешка* |
Обычно сохранены |
|
Снижение чувствительности и парестезии |
В зоне иннервации корешка* |
Отсутствуют |
|
Слабость и атрофия мышц |
В зоне иннервации корешка* |
Отсутствуют |
|
Возможные причины |
Грыжа диска |
Функциональная блокада или нестабильность ПДС |
|
*Признаки не являются облигатными. |
||
Рис. 4. Локализация боли при миофасциальном синдроме.
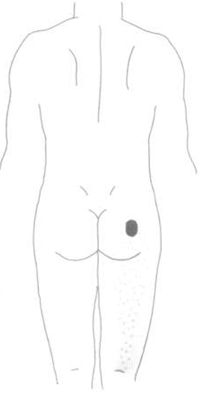
Таблица 2. Признаки, указывающие на необходимость тщательного обследования
Начало стойкой боли в спине в возрасте до 15 и после 50 лет
Немеханический характер боли (не уменьшается в покое, в положении лежа или в определенных позах, в ночное время)
Постепенное нарастание боли
Указание в анамнезе на злокачественное новообразование
Указание на возможность снижения иммунитета и склонность к повторным инфекциям
Возникновение боли на фоне лихорадки, снижения массы тела или других системных проявлений
Длительная скованность по утрам
Признаки поражения спинного мозга или конского хвоста (параличи, обширные зоны нарушения чувствительности, тазовые нарушения)
Изменения в анализе крови, мочи или других лабораторных тестах
Таблица 3. Основные НПВС, применяемые при лечении боли в спине
Препарат |
Способ применения/дозы |
Анальгетический эффект |
Вероятность побочного действия |
Примечание |
|
Диклофенак |
Внутрь 75–150 мг/сут в 1–3 приема В/м или в/в 75 мг 1–2 раза в день3–5 дней Ректально 50–100 мг 1–2 раза в день |
+++ |
++ |
Препарат выбора при выраженном болевом синдроме |
|
Ибупрофен |
Внутрь 200–600 мг 3 раза в день |
++ |
++ |
Препарат выбора при умеренной боли |
|
Индометацин |
Внутрь 25–50 мг 3–4 раза в сутки(максимум до 200 мг/сут) Ректально 50–100 мг 1 раз в день |
++ |
+++ |
Частые побочные эффекты; отрицательно влияет на метаболизм хряща; может вызывать психические нарушения у пожилых |
|
Кетопрофен |
Внутрь 100–320 мг/сут в 1–3 приема В/м 100–160 мг 1 раз в день Ректально 100–160 мг 1 раз в день |
+++ |
++ |
При применении высоких доз нередко возникают диарея, метеоризм, тошнота |
|
Кеторолак |
Внутрь 10 мг 2–4 раза в день В/м 30 мг 2–3 раза в день |
+++ |
+++ |
По анальгетическому эффекту сопоставим с наркотическими анальгетиками. Риск побочного действия возрастает при регулярном приеме свыше 7 сут |
|
Лорноксикам |
Внутрь 16–24 мг в первые сутки, затем 8 мг 2 раза, в/в или в/м 8–16 мг, далее 8 мг 2 раза в день |
+++ |
++ |
С осторожностью использовать при заболеваниях желудочно-кишечного тракта, почек, печени, у пожилых |
|
Мелоксикам |
15 мг 1 раз в сутки |
++ |
+ |
То же |
|
Пироксикам |
Внутрь 40 мг в первые сутки, затем 10–20 мг 1 раз в сутки Ректально 10–20 мг 1–2 раза в день |
++ |
++ |
Медленное начало действия (через 2–4 ч) |
|
Целекоксиб |
100 мг 2 раза в сутки |
++ |
+ |
Показан при наличии в анамнезе указаний на язвенную болезнь или НПВС-гастропатию |
|
Примечание. В/м – внутримышечно, в/в – внутривенно. |
||||
Рис. 5. Примерный алгоритм лечения острой боли в спине.
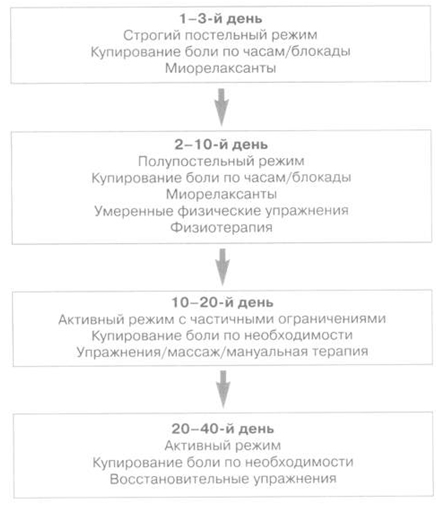
Таблица 4. Оценка эффективности терапии острой и хронической боли в спине с позиций доказательной медицины (на основе данных Tulder, Koes, 2003; Assenelft и соавт., 2003; Сherkin и соавт., 2003)
|
Методы лечения |
Оценка |
|
|
острая боль |
хроническая боль |
|
|
НПВС |
+ |
± |
|
Миорелаксанты |
+ |
± |
|
Антидепрессанты |
- |
? |
|
Постельный режим |
- |
- |
|
Физические упражнения |
+ |
+ |
|
Массаж |
? |
+ |
|
Мануальная терапия |
± |
± |
|
Физиотерапия |
? |
? |
|
Вытяжение |
± |
- |
|
Блокады |
+ |
± |
|
Акупунктура |
± |
? |
|
Примечание. "+" – положительное влияние, "±" – возможен кратковременный положительный эффект или данные противоречивы, "?" – отсутствуют надежные данные, "-" – положительный эффект отсутствует. |
||
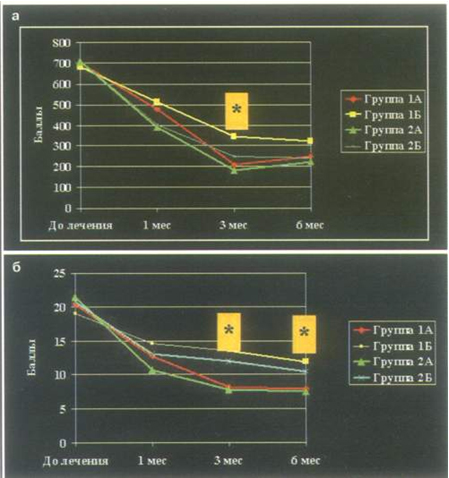
Рис. 6. Динамика самочувствия больных (а) и выраженности вертебрального синдрома (б) на фоне введения алфлутопа внутримышечно (группа 1А) и паравертебрально (группа 2А) и плацебо (соответственно группы 1Б и 2Б).
Психогенная боль в спине
Тревога, депрессия или другие психические изменения чаще всего лишь усиливают боль вертеброгенного происхождения, но иногда являются непосредственной причиной хронической боли в спине и ногах. Для психогенной боли характерна диффузность, нелокализованность. При осмотре слабость или онемение также выявляются во всей конечности и не укладываются в анатомические зоны иннервации, болезненность носит поверхностный характер (болезненны кожные покровы) или отмечается в необычных местах (например, над крестцом). Для выявления психогенной боли прибегают к специальным тестам. Например, больного просят встать коленями на стул и нагнуться вперед, в этом положении задние мышцы бедра расслабляются и больной с вертеброгенным болевым синдромом может наклониться довольно низко, тогда как больной с психогенной болью не может выполнить даже легкий наклон. При проверке симптома Ласега в положении сидя больные с психогенной болью, которые демонстрировали неспособность поднять ногу выше нескольких градусов, могут полностью выпрямить больную ногу. Следует учитывать, что наличие признаков психогенной боли не всегда исключает реальное физическое заболевание (например, грыжу диска), так как органические и психогенные факторы могут сочетаться [8].
Диагноз
Можно выделить два основных этапа в диагностике боли в спине. На первом этапе следует исключить заболевания, требующие специфической терапии, в частности опухоли, инфекционные и воспалительные поражения позвоночника, остеопороз и др.
Признаки, указывающие на необходимость особенно тщательного обследования пациента с целью выявления заболевания, требующего специфической терапии, приведены в табл. 2.
При наличии этих признаков необходимо тщательное дополнительное обследование. Основная задача рентгенографии позвоночника – исключить травматические или патологические переломы, врожденные аномалии, инфекционные или воспалительные заболевания, первичные или метастатические опухоли. Она показана всем больным с травмой, стойким болевым синдромом, а также при направлении на физио- или мануальную терапию. Часто рентгенография необходима, чтобы убедить больного в доброкачественности его заболевания. Люмбализация, сакрализация, spina bifida обычно не являются непосредственной причиной болей в спине. Не являются причиной боли и грыжи Шморля (грыжа диска в тело выше или ниже лежащего позвонка), но они могут служить индикатором дегенеративного процесса в позвоночнике.
Компрессионный перелом без указаний на травму может свидетельствовать о метаболическом остеопорозе, инфекции или опухоли. Однако опухоль или спондилит выявляется на рентгенограмме лишь в том случае, если произошла деструкция более 50% костной ткани. Поэтому если клинические данные заставляют заподозрить опухоль или спондилит, а рентгенография позвоночника не выявила патологии, то показаны радиоизотопная сцинтиграфия, КТ или МРТ. КТ лучше выявляет патологию костной ткани и позволяет диагностировать грыжу диска и стеноз позвоночного канала. МРТ более чувствительна к изменениям мягких тканей, в частности она хорошо выявляет изменение структуры диска (по изменению интенсивности сигнала от него), локализацию и размеры грыжи диска, позволяет исследовать состояние спинного мозга и конского хвоста, область межпозвонкового отверстия и более чувствительна к инфекционным и опухолевым поражениям позвоночника, патологии оболочек спинного мозга, аневризме аорты. На МРТ или КТ следует обязательно направлять больных при наличии признаков сдавления спинного мозга или конского хвоста.
При интерпретации данных КТ и МРТ важно учитывать, что примерно у 2/3 лиц, никогда не испытывавших боли в спине, эти методы исследования выявляют дегенеративные изменения в позвоночника, нередко на нескольких уровнях. Таким образом, обнаружение грыжи диска, проявлений спондилеза и стеноза позвоночного канала еще не означает, что именно они ответственны за имеющиеся у больного неврологические расстройства. Обязательным условием диагностики того или иного варианта вертеброневрологической патологии является соответствие клинических и параклинических данных.
При подозрении на сдавление спинного мозга или конского хвоста (если КТ или МРТ недоступны), а также при планировании оперативного вмешательства проводят миелографию. Другие исследования (рентгенографию легких, ультразвуковое исследование органов брюшной полости и малого таза, забрюшинного пространства, экскреторную урографию, ректороманоскопию и т.д.) проводят по показаниям.
Лечение острой боли в спине
При острой боли подход к лечению, по крайней мере на начальном этапе, менее дифференцирован. Алгоритм лечения острой боли в спине представлен на рис. 5. При острой люмбалгии и некорешковой люмбоишиалгии следует ожидать значительного уменьшения боли в течение 2–4 нед. В ряде контролируемых исследований показано, что постельный режим не только не ускоряет восстановление, но, наоборот, может способствовать хронизации болевого синдрома. Поэтому при умеренной боли необходимости в постельном режиме нет, а при интенсивной боли его следует максимально ограничить (до 1–3 дней). Затем режим расширяют, но рекомендуют на определенное время несколько ограничить физическую активность (в частности, избегать поднятия тяжести и длительного сидения). Больного следует научить, как правильно совершать движения, не увеличивая нагрузку на позвоночник. Раннее возвращение к привычному для больного уровню двигательной активности способствует более быстрому купированию боли и предупреждает ее хронизацию [4, 8].
Адекватное медикаментозное купирование боли не только облегчает состояние в данный момент, но также позволяет пациенту быстрее вернуться к привычному для него уровню повседневной активности, что в большинстве случаев имеет критическое значение для разрешения обострения. Аналгезирующие средства обычно достаточно назначить коротким курсом. Для облегчения боли применяют анальгетики (от парацетамола до трамадола и других наркотических средств) и/или нестероидные противовоспалительные средства (НПВС) внутрь, в виде ректальных свечей или внутримышечно (табл. 3). В первые дни лечения их предпочтительнее использовать профилактически – по часам, не дожидаясь усиления боли.
Следует отметить индивидуальную чувствительность больных к НПВС, в связи с этим при неэффективности оптимальных терапевтических доз одного из препаратов в течение 1–2 нед может быть испробован другой препарат. Облегчению боли могут также способствовать холод или легкое сухое тепло, тогда как глубокое или сильное прогревание чаще ее усиливает. Воздействие на мышечно-тонический компонент боли предполагает постизометрическую релаксацию, массаж и лечебную гимнастику, включающую упражнения на укрепление мышечного корсета или растяжение спазмированных мышц, применение миорелаксантов (клоназепама, тизанидина, баклофена), обычно не дольше 2 нед. Воздействие на вертеброгенный компонент боли включает методы мануальной терапии и лечебной гимнастики. При фасеточном синдроме паравертебрально проводят двустороннюю блокаду фасеточных суставов (иногда на нескольких смежных уровнях). Эти методы можно сочетать с рефлексотерапией, другими физиотерапевтическими процедурами (ДДТ, СМТ, электрофорез с местными анестетиками, фонофорез с гидрокортизоном и т.д.).
При корешковом синдроме сроки восстановления удлиняются до 6–8 нед. Принципы лечения остаются теми же – постельный режим в течение нескольких дней, анальгетики и НПВС, лечебная гимнастика. Особенность лечения состоит в более широком применении лечебных блокад и средств, воздействующих на невропатическую боль, в том числе антидепрессантов (например, амитриптилина) и антиконвульсантов (например, карбамазепина).
Если больной лечится в стационаре, то в остром периоде целесообразны эпидуральные блокады. Мануальная терапия при острой боли в спине может способствовать более быстрому восстановлению, однако в остром периоде грыжи диска, особенно при наличии признаков компрессии корешка, она противопоказаоказана. Хотя на практике применяют различные варианты вытяжения, убедительных данных в пользу его эффективности нет. В резистентных случаях при грыже диска иногда прибегают к ферментативному лизису диска с помощью внутридискового введения химопапаина.
Оперативное вмешательство показано: 1) при остром сдавлении конского хвоста, вызывающем развитие нижнего парапареза и тазовых нарушений; 2) при сдавлении корешка, вызывающего нарастающий парез; 3) при тяжелом инвалидизирующем болевом синдроме, не поддающемся консервативному лечению.
Лечение хронической боли в спине
Универсально эффективных методов лечения хронической боли в спине нет (табл. 4). НПВС, миорелаксанты, лечебные блокады, способствующие купированию острой боли в спине, при хронической боли малоэффективны и показаны лишь при ее обострениях [4]. При лечении хронической боли подход должен быть максимально индивидуализированным и дифференцированным. Важно исключить серьезные причины болей (опухоли, инфекции, остеопороз), а у остальных – выявить максимальное количество факторов, способствующих хронизации боли: вертебральных, периферических (нейродистрофические изменения мышц и соединительнотканных структур), психологических, соматических.
Стратегическая цель лечения при хронической боли состоит не столько в купировании боли, сколько в постепенном увеличении двигательных возможностей больного. Лечение должно в первую очередь включать немедикаментозные методы: мероприятия по снижению массы тела, лечебную гимнастику, массаж. Следует не только укрепить мышцы спины и брюшного пресса, что обеспечивает правильное распределение нагрузки на позвоночник, но и научить больного избегать провоцирующих движений, изменить его двигательный стереотип, провести коррекцию осанки.
На практике широко применяют мануальную терапию, тракцию, физиотерапевтические, бальнеологические, рефлексотерапевтические методы. Хотя все методы способны привести к краткосрочному улучшению, их долгосрочная эффективность остается под вопросом, поскольку ее не удается доказать в контролируемых испытаниях. Важно, чтобы больной понимал суть своего заболевания и принимал активное участие в выборе программы лечения. Решающее значение часто имеет коррекция сопутствующих аффективных нарушений (в том числе с помощью длительных курсов антидепрессантов).
Низкая эффективность терапии хронической боли во многом объясняется недифференцированным подходом, не учитывающим ее непосредственные причины. Между тем при наличии стойкой дискогенной боли, нарушающей адаптацию, могут быть показаны манипуляции на диске (например, электротермоанулопластика) или оперативное лечение (передний спондилодез), при патологии фасеточных суставов – интраартикулярное введение стероидов или радиочастотная невротомия. Однако инвазивность этих методов и возможность серьезных побочных действий заставляет искать новые возможности консервативной терапии хронической боли в спине.
Применение хондропротекторов в лечении хронической боли в спине
Одним из важнейших факторов, предопределяющих тенденцию к хронизации боли в спине, является разрушение хрящевой ткани, вовлекающее как межпозвонковые диски, так и межпозвонковые суставы. Именно оно вызывает стойкие биомеханические нарушения, способствующие постоянному возобновлению болевого синдрома, и провоцирует дальнейшее прогрессирование патологического процесса в структурах позвоночника, замыкая порочный круг при остеохондрозе позвоночника.
В связи с этим в комплексном лечении остеохондроза позвоночника может быть целесообразным применение препаратов, стимулирующих продукцию основных компонентов хряща (прежде всего протеогликанов) в хондроцитах и тем самым способствующих замедлению дегенерации хрящевой ткани и восстановлению ее структуры (так называемых хондропротекторов). Их использование может замедлить текущий дегенеративный процесс в позвоночнике и преодолеть тенденцию к хронизации боли в спине. Опыт применения различных хондропротекторов (хондроитин-сульфата, глюкозамина, алфлутопа и др.) при дегенеративных поражениях суставов конечностей (остеоартрозе) показал, что они способствуют более быстрому купированию болевого синдрома, предупреждению повторных обострений, восстановлению подвижности пораженных суставов и даже увеличению толщины суставного хряща.
К сожалению, до недавнего времени отсутствовали контролируемые исследования, которые бы подтверждали эффективность хондропротекторов при остеохондрозе позвоночника. Проведенное нами двойное слепое исследование эффективности одного из хондропротекторов – алфлутопа – показало, что у больных с умеренной и выраженной вертеброгенной люмбоишиалгией, имеющей хроническое рецидивирующее или персистирующее течение, препарат способствует стойкому уменьшению болевого синдрома, увеличению подвижности позвоночника и расширению функциональных возможностей пациентов. Лечебный эффект алфлутопа проявлялся уже в течение первых 2 нед после курса лечения и нарастал в течение первых 3 мес после курса лечения. В то же время к концу 6-го месяца отмечена тенденция к истощению лечебного эффекта, требующая повторного назначения препарата (рис. 6).
Сравнение двух путей введения алфлутопа – внутримышечного и паравертебрального – показало, что при паравертебральном пути введения лечебный эффект проявляется быстрее, а резистентность к препарату наблюдается реже. Наиболее эффективным препарат оказался у пациентов, имевших клинические признаки спондилоартроза, менее четким был эффект у пациентов с радикулопатией.
Полученный нами опыт позволяет рекомендовать применение алфлутопа в комплексном лечении больных остеохондрозом позвоночника с корешковыми и некорешковыми болевыми синдромами как при обострении (паравертебрально по 1 мл в 4 точки на уровне двух смежных сегментов дважды в неделю или внутримышечно по 1 мл в течение 20 дней), так и при частичной или полной ремиссии (внутримышечно по 1 мл в течение 20 дней). С целью предупреждения обострений повторные курсы лечения желательно проводить 2–3 раза в год.
Механизм действия препарата может объясняться его способностью угнетать активность гиалуронидазы, стимулировать биосинтез гиалуроновой кислоты – одного из основных компонентов хрящевой ткани и тем самым предотвращать разрушение макромолекулярной структуры основного вещества соединительной ткани и стимулировать процесс восстановления в хрящевой и околосуставных мягких тканях.
Литература
1. Богачева Л.А., Снеткова Е.П. Неврол. журн. 1996; 2: 8–12.
2. Веселовский В.П. Практическая вертеброневрология и мануальная терапия. Рига, 1991; с. 30–145.
3. Левит К., Захсе Й.Ю., Янда В. Мануальная медицина. М.: Медицина, 1993.
4. Попелянский Я.Ю., Штульман Д.Р. Болезни нервной системы. Под ред. Н.Н.Яхно, Д.Р.Штульмана. М.: Медицина, 2001; с. 293–316.
5. McCulloch J.A., Transfeldt E.E. Macnab’s Backache. Baltimore. Williams&Wilkins, 1997.
6. Попелянский Я.Ю. Ортопедическая неврология (вертеброневрология). М.: Медпресс-информ, 2003.
7. Bogduk N, McGuirk B. Medical management of acute and chronic low back pain. Amsterdam: Elsevier, 2002.
8. Waddel G. The back pain revolution. Edinburg. Churchill Livingstone, 1998.
9. Maigne R. Diagnosis and treatment of pain of vertebral origin. Baltimore. Williams&Wilkins, 1996.
10. Штульман Д.Р., Левин О.С. Неврология. Справочник практического врача. М.: Медпресс-информ, 2002; с. 70–90.
11. Вознесенская Т.Г. Боли в спине и конечностях. Болевые синдромы в неврологической практике. Под ред. А.М.Вейна. М.: Медпресс, 1999; с. 217–83.
12. Hall H. Back pain. J.H.Noseworthy (eds). Neurological therapeutics: principles and practice. London:Martin Dunitz, 2003.
Источник: http://www.consilium-medicum.com/media/consilium/04_08/547.shtml :: Wednesday, 10-Nov-2004 21:25:32 MSK













